1.1. Aminoácidos y péptidos
Los aminoácidos —unidades básicas que forman las proteínas— son compuestos que tienen todos ellos un grupo carboxilo (COOH) y un grupo amino (NH2) unidos al mismo átomo de carbono, denominado carbono α (alfa), diferenciándose en las cadenas laterales o grupos representados por R.
El carbono α de todos los aminoácidos, excepto en la glicina y la glicocola, es asimétrico, por lo que de cada aminoácido hay isómeros D y L, y son ópticamente activos.
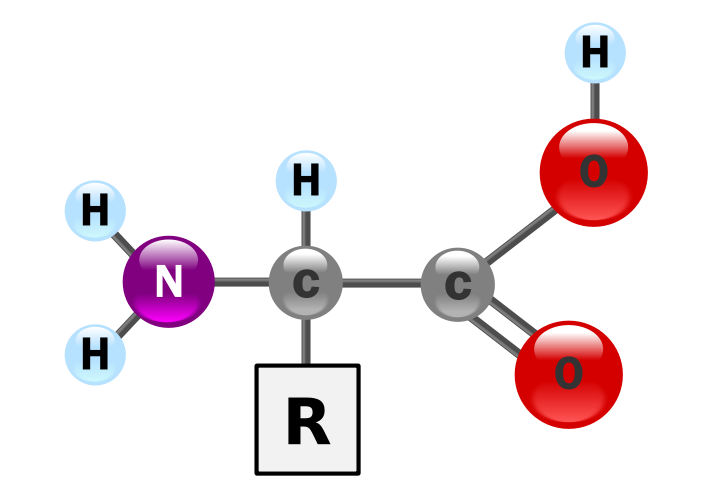 |
| Imagen 10. Autor: Yassine Mrabet. Dominio público |
Los radicales ácidos y aminos de los aminoácidos pueden ionizarse, por lo que su comportamiento es anfótero al convertirse en iones híbridos o zwiteriones, que se comportan como un par ácido-base que les permite hacer frente a los cambios de pH en el medio celular. El pH en el que tienden a adoptar la forma de dipolo eléctrico es distinto para cada aminoácido y se conoce como punto isoeléctrico.
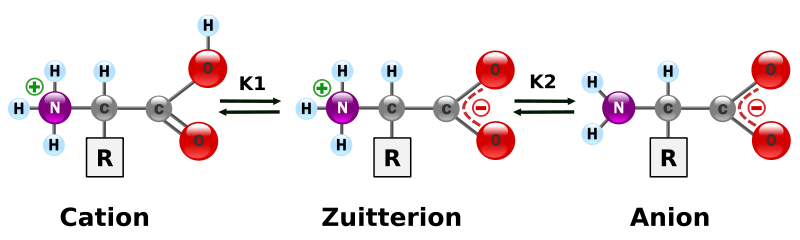 |
| Imagen 11. Autor: Yassine Mrabet. Dominio público |
Los aminoácidos son que tienen todos ellos un grupo (COOH) y un grupo (NH2) unidos al mismo átomo de , denominado carbono α ( ), diferenciándose en las laterales o R .
Clasificación de los α aminoácidos proteicos
La clasificación se basa en los grupos R, que en unos es polar e hidrófilo y en otros apolar e hidrófobo.
Se suelen hacer cuatro grupos:
- Neutros no polares o hidrófobos: carentes de grupos capaces de formar enlaces de hidrógeno, con igual número de radicales amino que carboxilo.
- Neutros polares sin carga: más solubles en agua que los no polares, porque sus radicales R pueden establecer puentes de hidrógeno.
- Ácidos: con mayor número de radicales carboxilo que amino, por lo que su carga neta es negativa.
- Básicos: con mayor número de radicales amino que carboxilo y con carga neta positiva.
Mira sus fórmulas
Los péptidos son compuestos formados por dos o más aminoácidos unidos mediante enlaces peptídicos.
El enlace peptídico es un enlace covalente entre el grupo amino de un aminoácido y el grupo carboxilo del otro, con desprendimiento de una molécula de agua. En el enlace peptídico, los átomos del grupo carboxilo y los del grupo amino se hallan en el mismo plano, con ángulos y distancias concretas, estabilizados por resonancia.
El enlace tiene carácter parcial de doble enlace, por lo que no permite giros como en los demás enlaces covalentes normales. Este hecho es determinante para la configuración espacial de las proteínas.
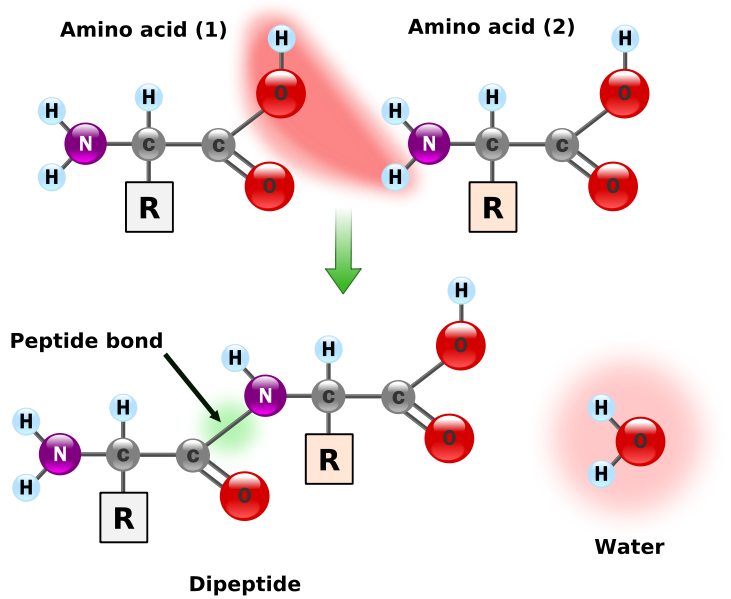 |
| Imagen 12. Autor: Yassine Mrabet. Dominio público |
¿Quieres ver esta explicación en una animación? Pincha en este enlace.
Verdadero Falso
Verdadero Falso
Verdadero Falso
Verdadero Falso