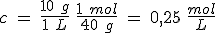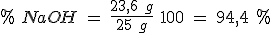1.3 Determinación de concentraciones y purezas
El objetivo de las valoraciones es determinar la concentración de una disolución, que puede llevar además a establecer la pureza de una muestra sólida.
Desde el punto de vista operativo, se trata simplemente de resolver un problema de estequiometría, teniendo en cuenta las cantidades de sustancia de ácido y de base que reaccionan.
El caso más sencillo, y muy frecuente, se da cuando reacciona un mol de ácido con un mol de base, como sucede con HCl y NaOH. Por tanto, n(HCl) = n(NaOH). Las cantidades de sustancia las expresarás como c V (concentración por volumen) si se trata de disoluciones, o como m/M (masa entre masa molar) si se trata de sólidos.
En otros casos, como sucede al reaccionar el H2SO4 o el Ca(OH)2, que producen dos iones H3O+ o dos iones OH-, simplemente deberás tenerlo en cuenta: si la reacción es entre NaOH y H2SO4, la neutralización es:
H2SO4 + 2 NaOH → Na2SO4 + 2 H2O
Por tanto, reaccionan dos moles de hidróxido por cada mol de ácido; es decir, n(NaOH) = 2 n(H2SO4).
|
8,37 g
| |
|
9,37 g
| |
|
10,37 g
| |
|
11,37 g
|