1. Propiedades del aire. Leyes de los gases perfectos.
- Es capaz de reducir su volumen cuando es
sometido a esfuerzos externos de compresión,
- igualmente cuando ocupa un recipiente elástico, se reparte uniformemente dentro de él
- y presenta un
coeficiente de viscosidad muy reducido por lo que tiene una gran facilidad de
fluir por las conducciones adecuadas.
Caudal, es la cantidad de aire
comprimido que atraviesa una sección de la conducción en la unidad de tiempo.
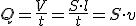
Donde:
| Q=caudal (m3/s) | S=sección (m2) |
t=tiempo (s) |
| V=volumen (m3) | l=longitud (m) | v=velocidad (m/s) |
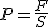
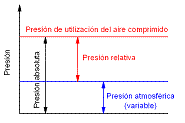
La presión se expresa de distinto modo, según el sistema de unidades utilizado:
- En el Sistema Internacional la unidad es: 1 Pascal=1N/1m2
- En el Sistema Cegesimal la unidad es 1 baria=1dina/1cm2, esta es una unidad muy pequeña por lo que se emplea un múltiplo que resulta ser: 1 bar=106 barias.
- En el Sistema Técnico la unidad es: 1kp/cm2.
En las aplicaciones neumáticas, según sean los autores de los textos, se emplean indistintamente cualquiera de las unidades, admitiéndose las siguientes equivalencias:
1bar = 1atm = 1kp/cm2 = 100KPa =105Pa.
La presión en la superficie de
|
|
 |
|
Imagen 01. Elaboración propia |
Imagen 02. wikipedia. Creative Commons |
Leyes de los gases perfectos
Haremos mención a las leyes que tienen más aplicación para el campo de la neumática, para lo que es necesario interpretar que el aire se comporta como un gas perfecto. Vamos a ver:
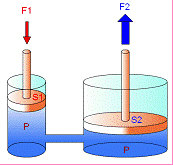
- El Principio de Pascal
- Ley de Boyle-Mariott
- Ley de Gay-Lussac
- Ley de Charles
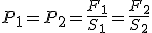
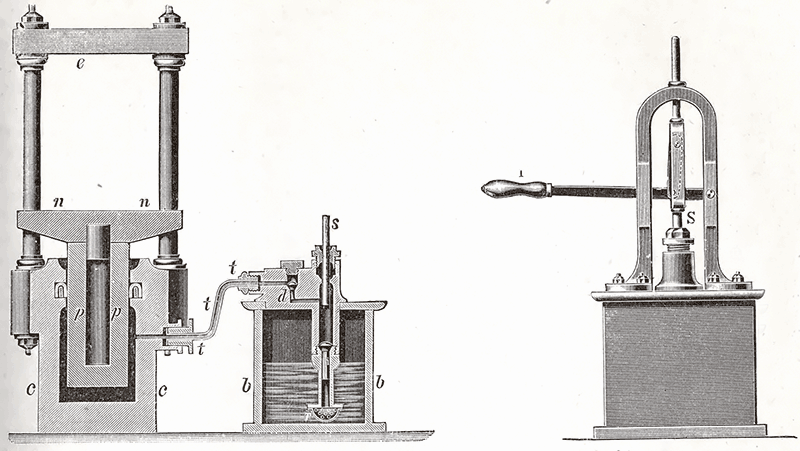
En esta
ley se basan las prensas hidráulicas.
 |
 |
|
Imagen 03. Elaboración propia |
Imagen 04. wikipedia. Creative Commons |
¿Qué fuerza se debe aplicar sobre un émbolo de 10 cm2 de superficie, de un circuito hidráulico, con el que se pretende elevar un automóvil de 1200 kg de masa, que se apoya sobre un émbolo de una superficie de 100 cm2?
En un taller se dispone de dos cilindros unidos mediante una tubería, las secciones de los pistones son: S1= 10 mm2 y S2 = 40 mm2. Si para levantar un objeto se le tiene que aplicar una fuerza F2=40 N sobre el pistón del segundo cilindro. ¿Cuál será la fuerza F1, que se tiene que realizar sobre el primer pistón?
En una prensa hidráulica, podemos realizar una fuerza máxima de 80 N. sobre el primer pistón, las secciones de los émbolos son de 40 cm2 y 200 cm2. ¿Cuál es la fuerza máxima que podrá desarrollar el segundo pistón?
Ley de Boyle-Mariotte, a temperatura constante, el volumen de un gas confinado en el interior de un recipiente rígido, es inversamente proporcional a la presión absoluta.
Es decir para una determinada cantidad de gas, el producto de la presión absoluta y el volumen, es una cantidad constante.
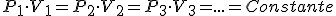
Ley de Gay-Lussac, si se mantiene la presión constante, el volumen ocupado por una determinada cantidad de gas es directamente proporcional a su temperatura absoluta, expresada en grados Kelvin, lo que se representa por la expresión:
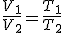
Ley de Charles, a volumen constante, la presión de una determinada cantidad de masa gaseosa es directamente proporcional a su temperatura absoluta, expresada en grados Kelvin, lo que se representa por la expresión:
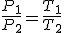
Todas las leyes anteriores se pueden resumir en la ecuación:
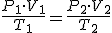
|
a) Cuanto ha aumentado la presión (expresada en bar)
b) Valor de la fuerza aplicada si el émbolo tiene una superficie de 100 mm2.