3. Enlace iónico
Formación de iones
Se forman iones por transferencia de electrones entre elementos metálicos y no metálicos: los primeros pierden electrones, formando iones positivos, y los segundos los ganan, dando lugar a iones negativos.
Formación de estructuras gigantes
Es importante que tengas en cuenta que no se forma un solo ión de cada tipo. Observa la animación, en la que verás que el único electrón de la capa más externa de un átomo de sodio pasa a completar la última capa de un átomo de cloro, conlo que los dos cumplen la regla del octete. Como puedes ver, se forma una gran cantidad de iones de ambos tipos, que interaccionan eléctricamente entre ellos, atrayéndose los de carga de distinto signo y repeliéndose los de carga del mismo signo. Todos esos iones se ordenan regularmente en una estructura gigante o cristal de forma cúbica, de manera que cuantos más iones se formen, porque se pone a reaccionar más cloro y más sodio, mayor será el cristal.
El tipo de ordenación de los iones se reproduce a escala macroscópica: observa los cristales de la imagen de la derecha, que tienen formas diferentes según sea la ordenación de los iones a escala microscópica.
|
|
 |
| Animación 2 Holger Schickor, uso educativo |
Imagen 13 Dr.T, Creative commons |
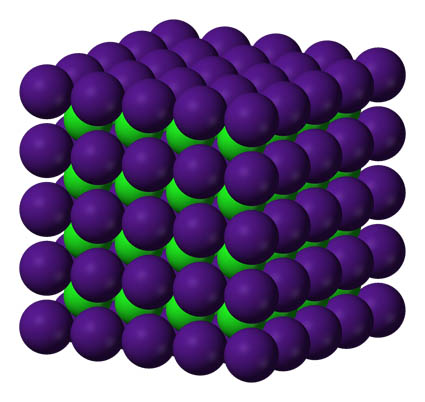
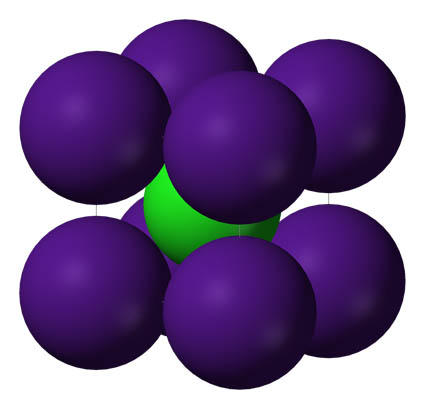
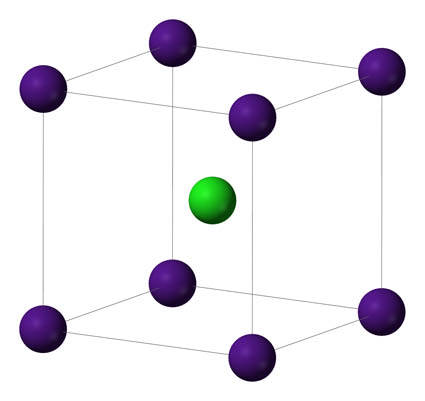
Fíjate en cómo se representan los diagramas de partículas de una sustancia iónica, el KCl. A la izquierda tienes la estructura de un trozo de sustancia, y en el centro y a la derecha, la unidad elemental que al repetirse da lugar a un cristal de KCl.
 |
 |
 |
| Imagen 14 Benjah-bmm27, Creative commons |
Imagen 15 Benjah-bmm27, Creative commons |
Imagen 16 Benjah-bmm27, Creative commons |
Significado de la fórmula de las sustancias iónicas
¿Qué significa la fórmula NaCl de la sal común, cuya formación acabas de ver? Evidentemente, no quiere decir que haya un solo ión de cada tipo, porque hay una gran cantidad de cada uno de ellos. La fórmula indica la proporción de iones en el compuesto: independientemente del tamaño del cristal, siempre hay el mismo número de iones Na+ que de Cl-.
Interpretación de las propiedades de las sustancias iónicas
Los iones se unen mediante intensas fuerzas electrostáticas. Por tanto, los puntos de fusión serán medios o altos (todas las sustancias iónicas son sólidas a temperatura ambiente), lo mismo que la dureza, ya que no es fácil separar iones. No conducen la corriente eléctrica en estado sólido, ya que los iones ocupan posiciones fijas en la red, pero sí lo hacen fundidos o en disolución, ya que en ese caso los iones tienen movilidad.
La reactividad de los metales alcalinos
En la historia inicial viste la gran reactividad de los metales alcalinos, capaces de reaccionar con el agua. ¿Qué sucede? Los átomos pierden un electrón, y con más facilidad cuanto más lejos está del núcleo, con lo que forman iones positivos para formar hidróxidos en una reacción muy violenta porque tienen una gran tendencia a producirse.
Ahora seguro que sabes por qué la reacción del litio se puede ver de cerca, mientras que en la del cesio es mejor alejarse todo lo que se pueda.
Sin embargo, la reacción del magnesio no tiene nada que ver. Hay que provocarla calentando a la llama, aunque cuando comienza se desprende una luz muy intensa, como ya viste en un vídeo en el tema 1 de la unidad 4. ¿Por qué razón? El magnesio tiene dos electrones en la capa más externa, y tiene menos tendencia a perderlos que si solamente tuviera que perder uno.
