2.1 Tipos de enlace y de estructuras
Hay dos mecanismos de formación de enlaces entre átomos, dependiendo de las configuraciones electrónicas de los átomos que se van a unir, relacionadas con su electronegatividad. Recuerda que un metal es un átomo con tendencia a perder los pocos electrones que tiene en la capa más externa, teniendo electronegatividad baja, mientras que los no metales tienen tendencia a ganarlos, ya que les faltan pocos para completarla, con lo que su electronegatividad es alta.
 |
 |
| Imagen 9 ChristianGlaeser, Creative commons |
Imagen 10 de elaboración propia |
Modelo para sustancias iónicas
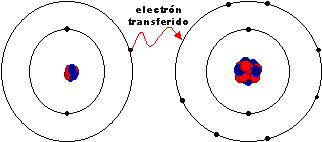
Si reacciona un metal con un no metal, se produce una transferencia de electrones desde los átomos que tienen que perderlos hasta los que necesitan ganarlos: el átomo que pierde electrones se transforma en un ión positivo (catión), mientras que el que los gana da lugar a un ión negativo (anión). Como son cargas de distinto signo, se atraen y se mantienen unidas. El enlace se llama enlace iónico.
Modelo para sustancias metálicas
Cuando los átomos son de metal, necesitan perder electrones, pero no hay átomos de no metal para ganarlos. El modelo de enlace es más complejo que el anterior y se llama enlace metálico.
Modelo para sustancias moleculares y sustancias covalentes
En el caso de ser átomos de no metal, necesitan electrones para cumplir la regla del octete. Pero como no hay átomos que los cedan, la única posibilidad que tienen es compartirlos. Como ves en la imagen, en lugar de que cada átomo tenga siete electrones, comparte uno con otro átomo, con lo que tiene seis electrones sin compartir y dos compartidos -ocho en total-; el enlace formado se llama enlace covalente.
Tipos de estructuras
Tanto las sustancias iónicas como las metálicas y las covalentes forman estructuras regulares tridimensionales, llamadas estructuras gigantes o cristales. Cuantos más átomos o iones hay, más grande es el cristal. La ordenación de las partículas a escala microscópica se reproduce a escala macroscópica, como puedes ver en el cristal de sulfato de cobre.
Sin embargo, en las sustancias moleculares hay un número finito de átomos unidos entre sí, dando lugar a partículas diferenciadas llamadas moléculas. En la imagen se muestra un modelo de molécula de etanol (alcohol etílico)
 |
 |
| Imagen 11 Stephanb, Creative commons |
Animación 1 JeanMi, Creative commons |
Tipos de enlace y de sustancia
En la imagen siguiente se resumen los tres tipos de enlace y los cuatro tipos de sustancia a que dan lugar, con dos ejemplos de cada uno de ellos.
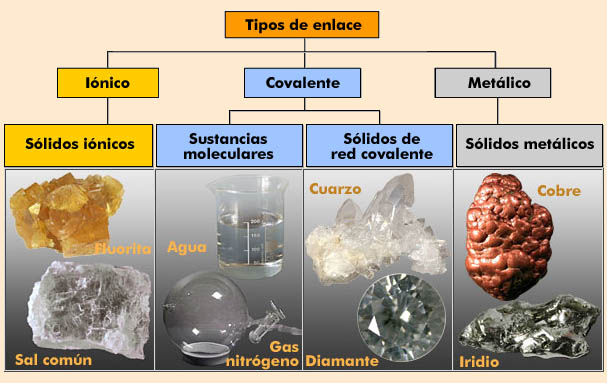 |
| Imagen 12 Mariano Gaite, uso educativo |