1.2 Variación de la concentración
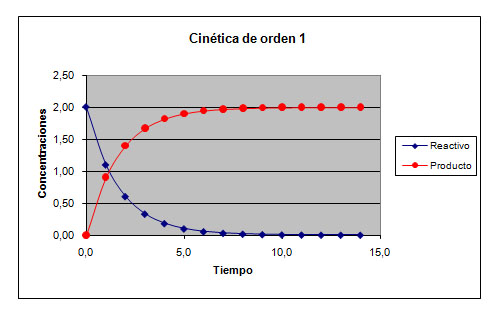 |
| Imagen 2 Elaboración propia |
También es muy interesante saber la concentración de reactivos que queda sin reaccionar después de un cierto tiempo de haber comenzado la reacción; es decir, disponer de una expresión del tipo [R]=f(t).
Si la cinética es de orden 1 en la reacción R → P, la expresión es [R]=[R]o.e-kt en la que [R] es la concentración del reactivo R a t unidades de tiempo después de haber comenzado la reacción, siendo [R]0 la concentración inicial del reactivo y k la constante de velocidad.
Fíjate en la gráfica. Verás que la reacción de desaparición de R es cada vez más lenta, con lo que el tiempo de reacción tiende a ser infinito: cuanto menos reactivo queda, más lentamente reacciona.
Como por cada mol de R se forma uno de P, la curva de evolución de la concentración de R es simétrica.
Vida media
El tiempo necesario para que la concentración de un reactivo se reduzca a la mitad recibe el nombre de vida media. Es una magnitud muy utilizada en otros campos de la ciencia que siguen cinéticas de orden uno, como por ejemplo en el estudio de la radioactividad.
Para calcularla, no tienes mas que sustituir en la ecuación general, teniendo en cuenta que [R]=[R]0/2.