1. Evolución de las ordenaciones periódicas
En 2010 se conocen 114 elementos, el último de ellos sintetizado en laboratorio en 2009, aunque hay noticias de que se han obtenido algunos átomos del elemento 117. ¡Cada vez es más difícil encontrar nuevos elementos! Solamente se consigue de vez en cuando en centros de investigación que disponen de aceleradores de partículas y tras procesos muy laboriosos (el laboratorio de Darmstadt, en Alemania, destaca por haberse descubierto en él los últimos elementos).
Piensa en que en 1250 se conocían apenas 10 elementos y que hubo que esperar hasta 1669 para conocer 14. En 1771 se llegó a los 20, y a 62 en 1868. En 1935, en pleno desarrollo de la mecánica cuántica ondulatoria, se alcanzaban los 88, y los 109 en 2006. Los últimos elementos se obtienen en cantidades muy pequeñas y pueden transcurrir años hasta que se reconocen definitivamente como nuevos elementos químicos.
Ordenaciones periódicas
Con la aplicación de las técnicas experimentales, en el siglo XIX se constató que había elementos químicos que tenían propiedades parecidas. De esta forma, comenzaron a proponerse ordenaciones de elementos que tenían propiedades similares (las triadas de Dobereiner, el caracol telúrico de Chancourtois y las octavas de Newlands).
 |
| Imagen 3 Sadi Carnot, Dominio público |
En 1869, El alemán Lothar Meyer y el ruso Dimitri Mendeleiev establecieron una ordenación de elementos por orden creciente de masa atómica, de manera que los elementos que estaban en la misma columna tenían propiedades físicas y químicas parecidas. Pero fue Mendeleiev el que publicó antes sus resultados y el que se ha llevado el reconocimiento universal.
En la imagen tienes esa primera ordenación, que es relativamente parecida a la tabla periódica que se utiliza en la actualidad.
Observa que hay dos elementos, de masas atómicas 68 y 70, que se indican con un interrogante. Eran elementos desconocidos entonces, pero que se descubrieron pocos años después. Observa la tabla y fíjate en la precisión de las previsiones de Mendeleiev, basadas en la repetición periódica de las propiedades.
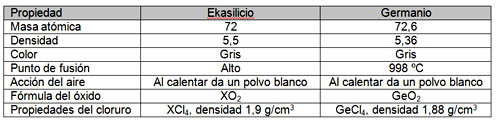
Éste fue su gran éxito y la razón por la que se le considera el padre de la tabla periódica.
Sin embargo, la tabla actual es diferente. Propuesta a principios del siglo XX, se debe a Werner y Paneth, tiene 18 columnas y 7 filas y los elementos ordenados por orden creciente de número atómico. La ordenación resultante difiere poco de la de Mendeleiev: hay tres parejas de elementos en los que un elemento está precedido por otro de masa atómica mayor, como es el caso del teluro, de masa relativa 127,6 y el iodo, de masa relativa 126,9.
Criterio de ordenación de elementos
El criterio de ordenación de elementos en la tabla periódica actual es el orden creciente de número atómico, de izquierda a derecha y de arriba a abajo debajo de manera que en la misma columna (grupo o familia) queden dispuestos los elementos con propiedades químicas parecidas.
Hay tres elementos descubiertos por españoles
En 1748 Antonio de Ulloa descubrió el platino en Colombia; en 1783 los hermanos Elhúyar aislaron el wolframio en Méjico, y en 1801 Antonio José del Rio descubrió en Méjico el vanadio (aunque recibió este nombre 30 años después).
|
| Imagen 4 Mardeg, Dominio público |
Acerca de la tabla periódica
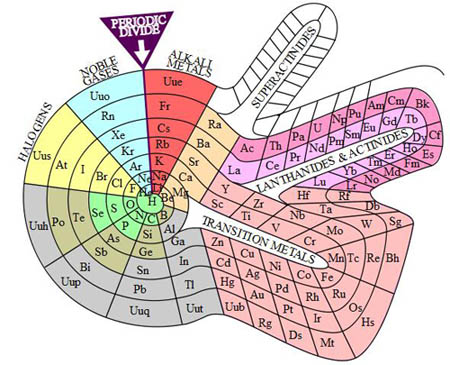
En la red hay multitud de sitios web relacionados con la tabla periódica, en los que hay información sobre aspectos interesantes tales como imágenes de cada elemento, usos que tienen, cuándo se descubrieron, etc, además de datos muy completos sobre las distintas clasificaciones realizadas hasta llegar a la tabla actual y nuevas propuestas como la que puedes ver en la imagen.
Dos de los más interesantes son los siguientes: