4. Ajuste de reacciones redox
El ajuste estequiométrico de los equilibrios redox implica a veces una gran dificultad cuando se pretende hacerlo mediante el método clásico, que es el que conoces (ir ajustando elemento a elemento entre reactivos y productos). Hay que tener presente que en un equilibrio redox no sólo existe una transformación de sustancias, sino también una transferencia electrónica de unas a otras.
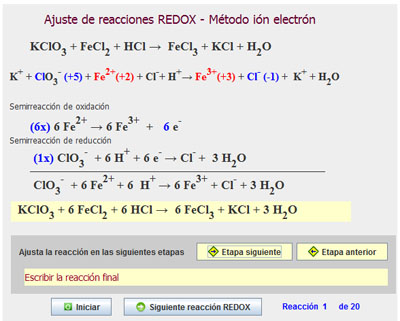
El método de ajuste que vas a utilizar se llama método del ion electrón. Se basa en que la reacción redox puede ser separada en dos semirreacciones, una de oxidación y otra de reducción, algo que realmente se puede hacer experimentalmente, como verás en el tema siguiente al ver cómo funcionan las pilas.
 |
| Imagen 9 Elaboración propia |
Etapas en el ajuste:
1. Determinar la variación de los números de oxidación.
2. Escribir la disociación iónica e identificar los agentes oxidantes y reductor.
3. Plantear las semirreacciones redox.
4. Ajustar la masa y la carga eléctrica en las semirreacciones.
5. Igualar el número de electrones cedidos y tomados.
6. Sumar las semirreacciones.
7. Ajustar las especies químicas que no intervienen.
En el simulador siguiente tienes la aplicación de este método a la resolución de 20 ecuaciones redox, tanto en medio ácido como básico.
Necesitas conexión a Internet para poder utilizarlo. Pulsando sobre la imagen de la derecha se abre una ventana nueva con el simulador. Puedes ver unas cuantas reacciones, y volver en otro momento. Ten en cuenta que cada vez se inicia la lista en una reacción diferente.
Ajustando reacciones redox
Hay muchas páginas con ejercicios de ajuste de reacciones redox. Esta página de Educaplus te resultará útil para practicar.
|
1, 6, 14, 2, 3, 7
| |
|
1, 9, 14, 1, 1, 7
| |
|
2, 8, 26, 2, 9, 14
| |
|
1, 2, 14, 2, 1, 7
|