1.1 Reacciones reversibles
Es importante que tengas una idea cualitativa de cómo se alcanza el estado de equilibrio. Para ello, vas a trabajar ahora con otros dos procesos. Tienen unas instrucciones en un inglés muy sencillo.
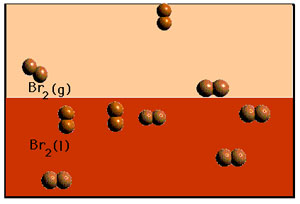
En primer lugar, fíjate en la simulación de la evaporación del bromo, y cuenta el número de partículas que hay en cada estado. Observa que se mantiene constante a lo largo del tiempo, a pesar de que las partículas van pasando de uno a otro estado.
El caso que realmente interesa analizar es el estado de equilibrio en las reacciones químicas. En la otra simulación puedes ver cómo se alcanza la situación de equilibrio en la reacción del formación del gas NO (monóxido de nitrógeno).
Fíjate en que quedan sin reaccionar tanto nitrógeno como oxígeno, y que continuamente reaccionan formando NO, mientras que éste se disocia regenerando N2 y O2. Observa que se pierde el concepto de reactivo y de producto, porque todas las sustancias son a la vez reactivos y productos, aunque por tradición y simplicidad se suele llamar reactivos a las sustancias que se escriben a la izquierda de la ecuación química, y productos a las que se escriben a la derecha.
Precisamente se llaman reacciones reversibles por esta razón: en el estado de equilibrio hay una mezcla de "reactivos" y "productos", y se alcanza ese estado partiendo de unos, de otros o de una mezcla de ambos.
 |
|
| Simulación 3 Greenbowe, Uso educativo |
Simulación 4 Proyecto TIGER, Uso educativo |
|
Se ha consumido todo el oxígeno inyectado en el recipiente.
| |
|
Se podría haber alcanzado el equilibrio inyectando solamente NO.
| |
|
Se trata de un proceso irreversible, que se indica con una sola flecha.
| |
|
En el estado de equilibrio es algo más rápida la síntesis del NO que su descomposición.
|
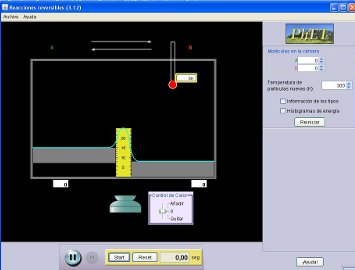
Simulador de reacciones reversibles
 |
| Simulación 5 Proyecto Phet, Creative commons |
Es interesante que utilices este simulador de reacciones reversibles, que permite que interacciones con él modificando varios parámetros y viendo la situación de un número elevado de moléculas.
Puedes cambiar el número de partículas que hay al comienzo de la experiencia, la energía que tienen al introducirlas (temperatura de las partículas nuevas), la energía libre de unas y otras y la energía de activación, suiendo o bajando los niveles respectivos.
También puedes suministrar energía en forma de calor para ver cómo afecta a la mezcla.
Experimenta probando con diferentes cantidades de partículas, observa cómo se llega al estado de equilibrio, cambia la energía de activación, etc. Lo importante es el concepto visual que vas a adquirir del equilibrio.