3.2 Derivados del petróleo y sus reacciones
Como se ha indicado, el petróleo está formado principalmente por hidrocarburos. Como estudiaste en el tema dedicado a la formulación de los compuestos del carbono, estos pueden ser de dos tipos: hidrocarburos saturados e hidrocarburos insaturados.
1) Hidrocarburos saturados
También denominados alcanos, son aquellos cuyos enlaces están completamente ocupados por átomos de hidrógeno. Los alcanos son poco reactivos debido a su escasa polaridad y a la estabilidad de sus moléculas, pero presentan una reacción característica:
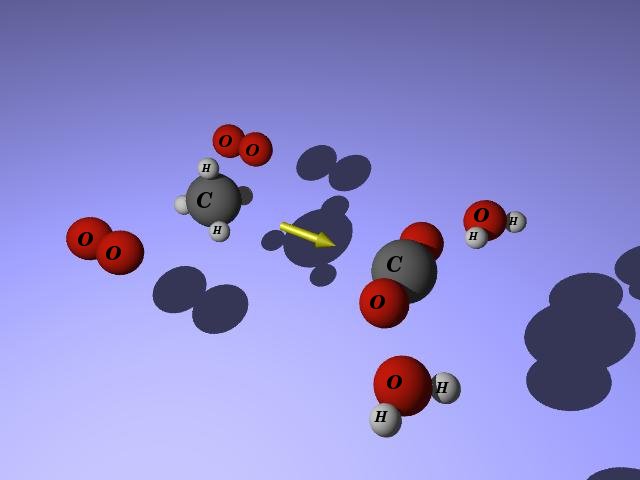 |
| Imagen 23. D. Gaya, dominio público |
Los alcanos presentan reacciones de combustión, en las que se combinan con oxígeno para dar lugar a dióxido de carbono y agua:
alcano + O2 → CO2 + H2O
La característica fundamental de las reacciones de combustión es que liberan gran cantidad de energía en forma de calor, esto es, son altamente exotérmicas, por lo que históricamente han sido utilizados como combustible. Ejemplos de ello son el metano, el propano o el butano.
2) Hidrocarburos insaturados
Son aquellos que presentan dobles (alquenos u olefinas) o triples enlaces (alquinos). Son mucho más reactivos que los alcanos ya que las insaturaciones (enlaces múltiples) provocan que la cadena sea más inestable. Presentan reacciones de combustión al igual que los alcanos, pero reaccionan fácilmente con el hidrógeno o con los halógenos, en reacciones de adición:
Los alquenos y alquinos son fácilmente, además de combustión, experimentan reacciones de adición al doble o triple enlace.
En estas reacciones el hidrógeno (H2), un halógeno (X2) o un hidrácido (HX) se unen al hidrocarburo insaturado en el enlace múltiple, formando un único producto con dos nuevos enlaces.
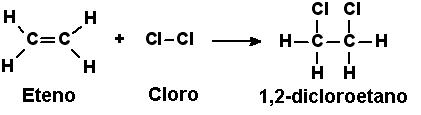 |
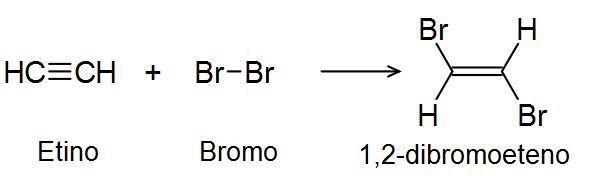 |
| Imagen 24. Elaboración propia |
|
Los alquinos normalmente reaccionan en dos etapas, la primera para dar lugar a un alqueno y la segunda al producirse otra adición en este para dar lugar a un alcano.
En una reacción de polimerización los compuestos de carbono de bajo peso molecular (denominados monómeros) se unen químicamente entre sí para formar una molécula larga en forma de cadena, denominada polímero.
Un polímero típico consta de miles de estos monómeros.
En la siguiente animación puedes ver la formación de un polímero a partir de un monómero. Para comenzar debes presionar el botón verde de Play. Observa cómo se forma la cadena y se marcan los puntos de anclaje en cada extremo con estrellas rojas. En esos puntos se seguirían enlazando más monómeros hasta dar lugar al polímero final.
|
|
| Animación 3. Flashlearning Uso libre |
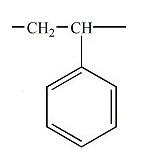
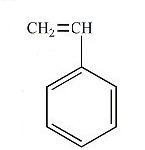
Al finalizar la animación, presionando los botones de colores de la parte inferior, tienes la opción de observar la estructura de algunos de los polímeros más sencillos como el polietileno, del que es monómero el eteno -también conocido como etileno- (botón verde) o el poliestireno (botón naranja).
Existen tanto polímeros naturales como artificiales. Dentro de los naturales destacan la molécula de ADN, la lana, la seda o la celulosa. Entre los artificiales, que comenzaron a sintetizarse a mediados del siglo XIX, el poliestireno, poliuretano o el nylon.
El poliestireno es un polímero que se utiliza principalmente para producir envases y, sobre todo, como aislante térmico en construcción. En la imagen se muestra un fragmento de poliestireno expandido, llamado habitualmente poliexpan o porexpan, que seguro que identificas.
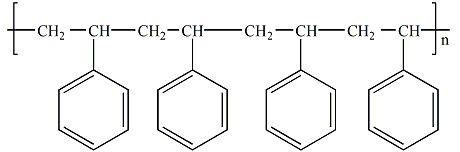
Su estructura química es la que se muestra a continuación:
 |
|
| Imagen 25. Dominio público |
Imagen 26. Vmadeira, Creative Commons |
Dibuja el monómero del poliestireno a partir de la estructura anterior.