3. Preparación de disoluciones
¿Qué debes hacer para preparar una disolución con la composición que te interese?
Vas a ver el procedimiento para preparar 250 mL de disolución de NaCl (sal común) de concentración 0.4 mol/L. En el vídeo tienes detallados los pasos fundamentales.
|
|
|
| Video 1 de elaboración propia |
Imagen 9 de CNICE, uso educativo |
1. Prepara el material necesario: balanza, vidrio de reloj, espátula, vaso de precipitados, varilla, matraz aforado, frasco lavador con agua y sustancia a disolver (NaCl en este caso).
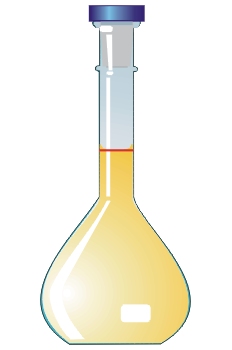
2. Haz los cálculos oportunos para saber la masa de NaCl que hay que pesar:
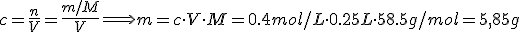
La balanza utilizada llega a medir 0.1 g, por lo que la pesada es de 5.9 g.
3. Coloca el vidrio de reloj en la balanza y táralo (la balanza marca 0, con lo que se descuenta el peso del vidrio).
4. Añade sal común con la espátula hasta que la balanza marque 5.9 g.
5. Pasa el sólido a un vaso de precipitados. Arrastra los últimos granos de sal con el frasco lavador, añadiendo un poco de agua sobre el vidrio.
6. Añade más agua al vaso de precipitados y agita hasta que se disuelva todo el sólido.
7. Pasa con cuidado la disolución al matraz aforado, aprovechando el pico del frasco lavador. Aclara dos o tres veces el vaso con el frasco lavador y añade el agua al matraz.
8. Completa con agua hasta el aforo, marca situada en el cuello del matraz que indica hasta dónde debe haber líquido para alcanzar la capacidad del matraz. Se suele hacer con un cuentagotas, o con el frasco lavador si se tiene una cierta costumbre.
Por último, se etiqueta el matraz con la sustancia y su concentración o se almacena en un frasco de vidrio, también etiquetado.
Un recipiente A contiene 2 litros de NaOH 2 mol/L. Otro recipiente B contiene 8 litros de NaOH 0.5 mol/L. Si se dejase evaporar el agua de las dos disoluciones ¿en cuál se recuperaría más hidróxido de sodio?
|
En la disolución A.
| |
|
En la disolución B.
| |
|
Igual en los dos casos.
|